Un avance para la neurociencia: Sanford Burnham y Singapur sacan sus cartas
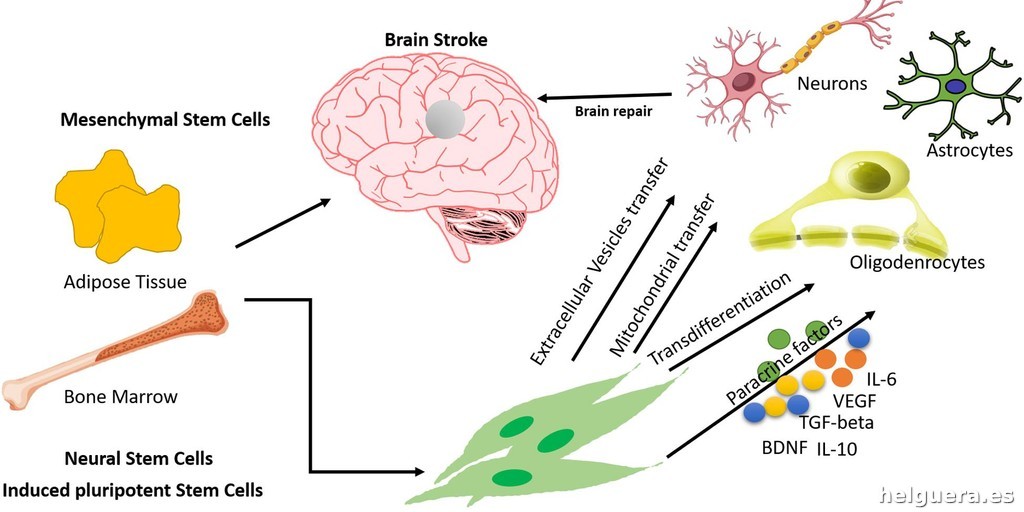
La historia más reciente de la regeneración cerebral tiene dos protagonistas con nombres serios: el Instituto Sanford Burnham Prebys de Descubrimiento Médico y la Facultad de Medicina de la Universidad Nacional de Singapur. A fecha de hoy, 2024, están rompiendo esquemas con un experimento que no es cualquier cosa: aprovechar células madre humanas para reparar regiones cerebrales dañadas por un ictus, usando cerebros de ratones vivos como campo de pruebas.
No es ciencia ficción, pero todavía no alcanza esa magia absoluta que imagina el público. Las células humanas se cultivan y luego se transplantan en el cerebro de ratones que han sufrido un ictus experimental. ¿Qué resulta? Parece ser que encontraron el cóctel ideal de moléculas pequeñas y proteínas estructurales que permiten que esas células madre se transformen en neuronas funcionales y, más importante, no se queden como un bulto muerto o huérfano en el tejido dañado. O sea, que no solo viven, sino que además, empiezan a reconstruir las conexiones perdidas, como si fueran arquitectos activos de un puente caído hace años.
Antes de que te aventures a gritar victoria, hay que aclarar que los resultados aún están en su fase más temprana (y preclínica) y los ratones, aunque excelentes modelos, no son humanos. Pero psicológicamente, tiene que ser un soplo de aire fresco para una comunidad científica que llevaba años atrapada en callejones sin salida, peleando contra un cerebro que simplemente no quiere repararse a sí mismo. Quizá esto sea lo que se conoce como “el primer paso de un largo camino”.
—
¿Por qué el cerebro es un enemigo para la regeneración post-ictus?
Córtate la idea de que las células cerebrales se tiran de los pelos y se reproducen como conejos cuando hay daño. La verdad cruda: el cerebro es más bien un mal hostal para células nuevas cuando sufre un ictus. Primero, porque un ictus corta el suministro de sangre en zonas cruciales, con las consiguientes muertes neuronales por falta de oxígeno y nutrientes.
Luego, el verdadero drama empieza cuando la tormenta se calma. La zona afectada está ahora repleta de moléculas inflamatorias —como si el cerebro te pusiera el cartel de “no pasar”— que reprimen la llegada y proliferación celular. A esto añádele la barrera física construida por la cicatriz glial, una especie de muro que el cerebro levanta para protegerse a sí mismo de más daños, pero que también entierra la esperanza de la regeneración.
El doble combo: ambiente tóxico químicamente y barreras físicas, hace que cualquier célula madre tenga que enfrentarse a una jungla esperando un zoológico en el que prosperar. Esta hostilidad ha sido un obstáculo grande para la tecnología de la medicina regenerativa, y es el motivo por el cual las pruebas con células madre hasta ahora no pasaban de promesas tibias.
—
De células madre a neuronas con propósito: la ciencia detrás del truco
Convertir células madre en neuronas no es exactamente un truco nuevo. La comunidad científica lleva años haciéndolo en laboratorio. El drama siempre ha sido llevar esas neuronas a la batalla real: el tejido cerebral lesionado y hostil. Ahí suelen moriras o quedar desconectadas, como si tirases ladrillos construidos para un puente sin planos que indiquen dónde poner cada uno.
Pero aquí es donde los equipos de Sanford Burnham y Singapur metieron mano y la liaron parda (en el buen sentido). Después de probar mil combinaciones, encontraron que un mix molecular específico, conformado por pequeñas moléculas y proteínas estructurales, facilitaba que las células madre se transformaran en neuronas funcionales que no solo sobrevivían, sino que se posicionaban correctamente en la zona daña y, sobre todo, empezaban a tender las redes nerviosas necesarias para comunicarse.
¿Y cómo saben que estas neuronas se conectan bien? Utilizaron un genoma etiquetado con códigos de barras genéticos que, como una lona fluorescente en la oscuridad, permite seguir cómo y dónde se expresan diferentes genes en estas células después del trasplante. Se pudo observar que cada neurona no solo sabe qué tipo celular es, sino hacia dónde debe enviar sus axones, formando conexiones específicas en distintas regiones cerebrales y hasta la médula espinal. Una especie de GPS molecular con instrucciones para reparar el cableado perdido.
—
¿Por qué parecía imposible que esto pasara?
La respuesta corta: el cerebro no es un Lego cualquiera. Pulir un clon celular parece sencillo hasta que tienes que hacer que no sólo viva, sino que funcione exactamente como una pieza en un sistema ultra-conectado y preciso.
Los intentos anteriores con células madre chocaban contra la cruda realidad de que las neuronas resultantes no se conectaban bien o directamente morían en la zona dañada. El problema no reside solo en generar células nuevas, sino en integrarlas con las viejas. Reconectar neuronas “a ninguna parte” no sirve de nada, salvo para aumentar la frustración y invertir recursos inútilmente.
Además, la rigidez del entorno cicatrizal actúa como una barrera física impenetrable y el entorno químico inflama y ahuyenta cualquier intento ingenuo que no tenga armas moleculares para enfrentarse a él. Era un callejón sin salida para proyectos que dejaban células en el cerebro esperando que la magia sucediera.
—
Proteínas que manipulan genes: el nuevo controlador del crecimiento neuronal
El hallazgo aún más interesante dentro del estudio fue descubrir que ciertas proteínas pueden controlar cómo se expresan los genes dentro de las neuronas recién nacidas. Esta regulación no es baladí, pues activa o desactiva genes claves que determinan el comportamiento de las neuronas, especialmente la manera en que ramifican sus axones y dendritas.
Este control genético molecular ofrece un mecanismo para “programar” neuronas que no solo existen, sino que se comportan de manera adecuada en el entorno cerebral remodelado tras un ictus.
Piénsalo: hasta ahora hablamos de células “activas”, pero ¿y si además les otorgas un software interno que les dice cómo actuar y a dónde ir? Eso cambia completamente las reglas del juego. Los científicos han dejado claro que sin esta orquestación molecular, todo el avance previo podría quedarse en nada, con neuronas que simplemente no forman las conexiones adecuadas.
—
Lo que esto implica para la medicina regenerativa: una esperanza pero con los pies en la tierra
Que un equipo logre que células humanas trasplantadas en ratones produzcan neuronas funcionales y con capacidad para reconstruir circuitos neuronales, suena más a big bang que a simple avance. Pero recordemos que esto es un paso inicial.
Queda demasiado camino por recorrer hasta que pueda replicarse en humanos. Problemas como el rechazo inmunológico, diferencias entre la complejidad cerebral humana y la de los modelos animales y la respuesta inflamatoria en pacientes (que suele ser una locura) son retos gigantescos que aún se esconden en la penumbra. ¿Pero es suficiente para ser optimistas? Sí.
Un ictus deja daños terribles y permanentes hoy. Las herramientas actuales en terapia post-ictus son limitadas y mayormente rehabilitativas, sin una verdadera solución para revertir la pérdida neuronal. Esta técnica abre la puerta para pensar no sólo en detener daños, sino en repararlos realmente.
—
¿Y ahora qué? ¿Estamos en la era del cerebro reparable?
Por primera vez, no se habla solo de trasplantes celulares o de esperanzas vagas, sino de entendimiento profundo del comportamiento genético de neuronas trasplantadas y su integración correcta en circuitos cerebrales dañados.
Esto podría convertirse en el futuro estándar para tratar lesiones neuronales, no solo por la precisión de la regeneración sino porque podría aplicarse a otras enfermedades neurodegenerativas, en teoría.
Ojo, porque los pasos para llegar a terapias humanas son complejos: necesitarán toneladas más de experimentos, ensayos clínicos, y superar obstáculos biológicos brutalísimos. Pero como primer paso real para decir «sí, se puede reconstruir el cerebro tras un ictus» es un bombazo.
No obstante, mejor no poner la carreta delante de los bueyes ni esperar milagros inmediatos. Los cerebros humanos son el final de la evolución en complejidad y, por tanto, son expertos en decir “no” a soluciones fáciles.
¿Pero tú qué opinas? ¿Te gustaría que los próximos años trajeran medicamentos basados en células madre capaces de reconectar tu cerebro como si nada? Porque, si se confirma, este podría ser el golpe más duro a la idea de que “una vez muerto, el cerebro no revive”.